Strona główna > Chemia > Chemia nieorganiczna > Reakcje redoks
Utleniacze to pierwiastki, których atomy mogą przyjmować elektrony. Utleniacz pobierając elektrony dokonuje utlenienia reduktora.
Reduktory to pierwiastki, których atomy mogą oddawać elektrony. Reduktor oddając elektrony dokonuje redukcji utleniacza.
Przykład reakcji redoks - reakcja kwasu azotowego (V) i miedzi
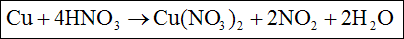
W trakcie tej reakcji zachodzi reakcja utlenienia miedzi:
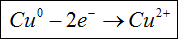
i redukcji azotu:
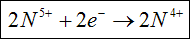
Miedź jest w tej reakcji reduktorem a azot utleniaczem.
Na poniższym filmie pokazujemy reakcję między miedzią i kwasem azotowym (V). W trakcie reakcji wydziela się trujący tlenek azotu (IV) NO2.
2013-03-23 19:21:26 Ol napisał(a):
Nie mogę nic znaleźć o manganie i chromie. jestem gapa, czy nie ma tego nigdzie?
Reakcje redoks
Reakcje redoks to inaczej reakcje utlenienia i redukcji. W trakcie ich przebiegu jedne atomy/jony utleniają się (zwiększają swój stopień utlenienia) a inne redukują się (zmniejszają swój stopień utlenienia).Utleniacze to pierwiastki, których atomy mogą przyjmować elektrony. Utleniacz pobierając elektrony dokonuje utlenienia reduktora.
Reduktory to pierwiastki, których atomy mogą oddawać elektrony. Reduktor oddając elektrony dokonuje redukcji utleniacza.
Przykład reakcji redoks - reakcja kwasu azotowego (V) i miedzi
W trakcie tej reakcji zachodzi reakcja utlenienia miedzi:
i redukcji azotu:
Miedź jest w tej reakcji reduktorem a azot utleniaczem.
Na poniższym filmie pokazujemy reakcję między miedzią i kwasem azotowym (V). W trakcie reakcji wydziela się trujący tlenek azotu (IV) NO2.
Zobacz artykuły, które mogą Cię zainteresować:
Dodaj komentarz do artykułu.
Komentarze użytkowników (1)
2013-03-23 19:21:26 Ol napisał(a):
Nie mogę nic znaleźć o manganie i chromie. jestem gapa, czy nie ma tego nigdzie?